L'osmose inverse expliquée
24 Mai 2023 | Par Cieléo | Filtration de l'eau

L’osmose inverse est une technique efficace et économique de purification de l’eau. C’est avant tout une technologie “naturelle” ayant pour base un principe, appelé l’osmose, mis en évidence en 1748 par Jean Antoine Nollet, abbé et physicien français. Son application technique, l’osmose inverse, a été développée aux U.S.A. par l'université de Californie et de Floride au milieu des années 1950 pour dessaler l’eau de mer et les eaux saumâtres. Elle est devenue depuis la méthode la plus performante de purification de l'eau.
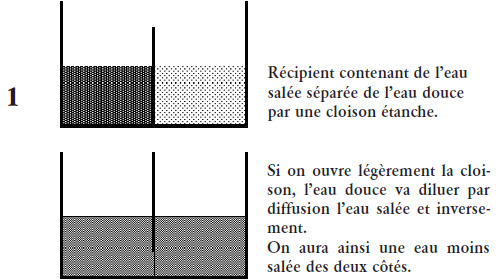
Prenons un récipient contenant de l’eau salée séparée de l’eau douce (1). Dès qu’on ouvrira légèrement la cloison, il y aura diffusion des liquides l’un vers l’autre de manière à obtenir un mélange homogène aussi salé des deux côtés.
Si maintenant on sépare eau douce et eau salée par une membrane semi-perméable (2), ne laissant passer que l’eau tout en retenant les substances solides dissoutes, et donc le sel, on peut alors observer que c’est l’eau douce qui traversera la membrane pour diluer la solution salée. Il y aura ainsi plus d’eau salée que d’eau douce.
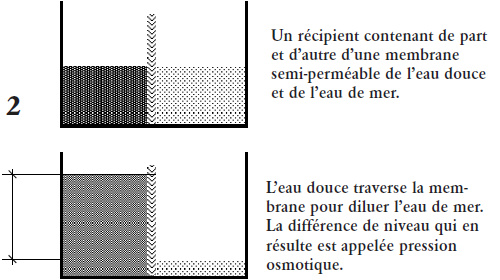
Ce phénomène de diffusion, appelé principe d’osmose, se produit quand deux solutions de concentrations moléculaires différentes se trouvent séparées par une membrane semi-perméable, laissant passer le solvant et non la substance.
La différence de niveau entre les deux liquides exprime la pression osmotique. Cette pression varie suivant la masse moléculaire et la concentration des solutions en présence.
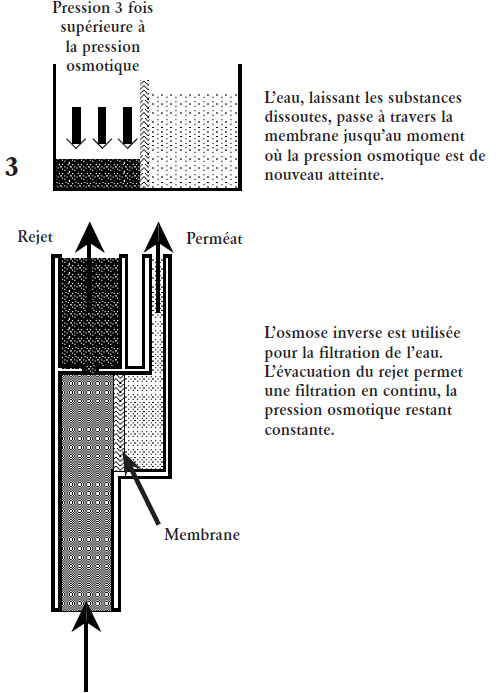
Si on applique une pression extérieure sur la solution salée, supérieure à sa pression osmotique (3), une partie de celle-ci traversera la membrane en se débarrassant de son sel. C’est ce que l’on appelle l’osmose inverse.






Ajouter un commentaire